Предмет: Химия,
автор: Аноним
вычислите и укажите массу раствора с массовой долей гидроксида натрия 25% которая израсходуется при переработке на мыло 200 кг стеариновой кислоты. Проверьте пожалуйста ошибки на фото
Приложения:
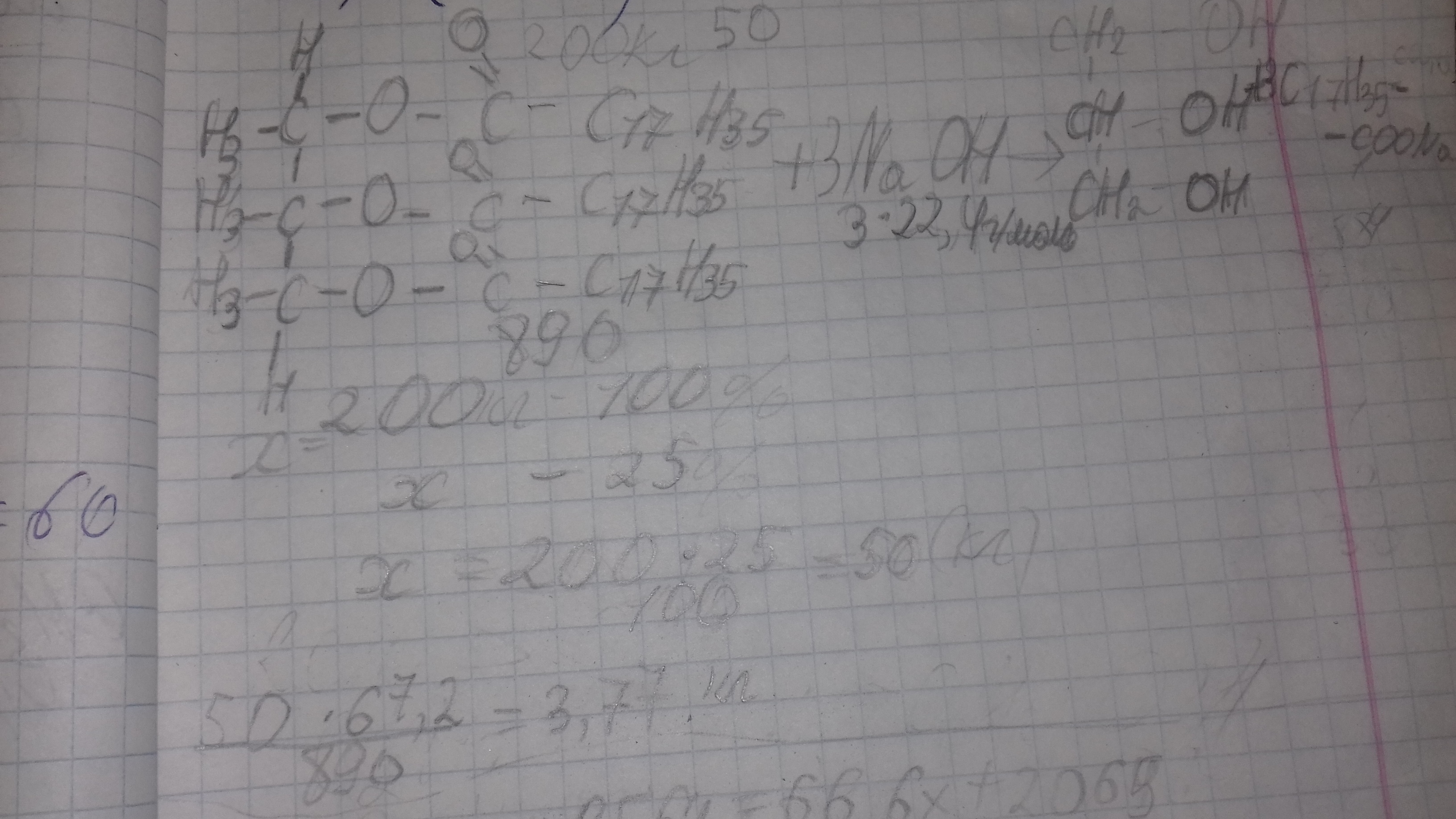
евакот3:
ответ 112 68
Ответы
Автор ответа:
17
ДАНО
m(C17H35COOH) = 200 kg
W(NaOH) = 25%
--------------------------------------
m(ppa NaOH)-?
200 kg Xkg
C17H35COOH+NaOH-->C17H35COONa+H2O
284 40
M(C17H35COOH)=284 kg/kmol , M(NaOH) = 40 kg/kmol
X = 200*40 / 284 = 28.17 kg
m(ppa NaOH) = 28.17*100% / 25% = 112.68 kg
ответ 112.68 кг
m(C17H35COOH) = 200 kg
W(NaOH) = 25%
--------------------------------------
m(ppa NaOH)-?
200 kg Xkg
C17H35COOH+NaOH-->C17H35COONa+H2O
284 40
M(C17H35COOH)=284 kg/kmol , M(NaOH) = 40 kg/kmol
X = 200*40 / 284 = 28.17 kg
m(ppa NaOH) = 28.17*100% / 25% = 112.68 kg
ответ 112.68 кг
я боюсь за себя , что будет в старших классах
а ты не бойся ,просто учись.
в смысле ?
даа
точно я не могу математику заделать Вы помогите мне
пожалуста
пака
Автор ответа:
17
Дано:
m(C17H35COOH) = 200 кг
w(NaOH) = 25%
Найти:
m(NaOH) -?
Решение
C17H35COOH + NaOH → C17H35COONa + H2O
M(C17H35COOH) = 284 г/моль
M(NaOH) = 40 г/моль
Составим пропорцию:
284 г -40 г
200 кг - х
х=28.17 кг - это масса NaOH ( не раствора)
Масса раствора:
w(NaOH) = m(NaOH)/m раствора(NaOH) *100%
m раствора (NaOH) = 28.17/0.25 = 112.68 кг
m(C17H35COOH) = 200 кг
w(NaOH) = 25%
Найти:
m(NaOH) -?
Решение
C17H35COOH + NaOH → C17H35COONa + H2O
M(C17H35COOH) = 284 г/моль
M(NaOH) = 40 г/моль
Составим пропорцию:
284 г -40 г
200 кг - х
х=28.17 кг - это масса NaOH ( не раствора)
Масса раствора:
w(NaOH) = m(NaOH)/m раствора(NaOH) *100%
m раствора (NaOH) = 28.17/0.25 = 112.68 кг
нор
нормально
спс
Интересные вопросы
Предмет: Литература,
автор: kripnastyaaa
Предмет: Обществознание,
автор: anyanafikovaoff
Предмет: Английский язык,
автор: tomenkomaya
Предмет: Математика,
автор: Lalok300123
Предмет: Литература,
автор: dfkthbz16021