Предмет: Химия,
автор: zheka566
70грамм 55%соляной кислоты взаимодействуют с нитратом серебра вычислить массу образующегося осадка
Ответы
Автор ответа:
1
решение задачи смотрите на фото.
Приложения:
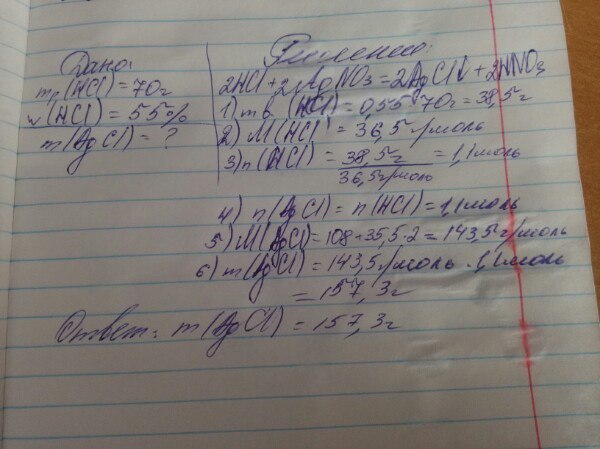
Автор ответа:
1
узнаем чистую массу соляной кислоты:
m(HCL)=70*(55:100)=38,5 грамм
составим формулу реакции:
HCl+AgNO3=AgCl+HNO3
хлорид серебра осадок
узнаем количество вещества кислоты
n(HCl)=38,5/(1+35)=1,1
n(HCl)=n(AgCl)=1,1
m(AgCl)=1,1*(108+35)=157,3грамм
m(HCL)=70*(55:100)=38,5 грамм
составим формулу реакции:
HCl+AgNO3=AgCl+HNO3
хлорид серебра осадок
узнаем количество вещества кислоты
n(HCl)=38,5/(1+35)=1,1
n(HCl)=n(AgCl)=1,1
m(AgCl)=1,1*(108+35)=157,3грамм
Интересные вопросы
Предмет: Математика,
автор: 88ag33
Предмет: Литература,
автор: Nikita22874
Предмет: Математика,
автор: sabinadubrovina122
Предмет: Биология,
автор: school1151
Предмет: Алгебра,
автор: and444and