Предмет: Математика,
автор: lplrmila
реши уравнения 12:x+10=13
Приложения:
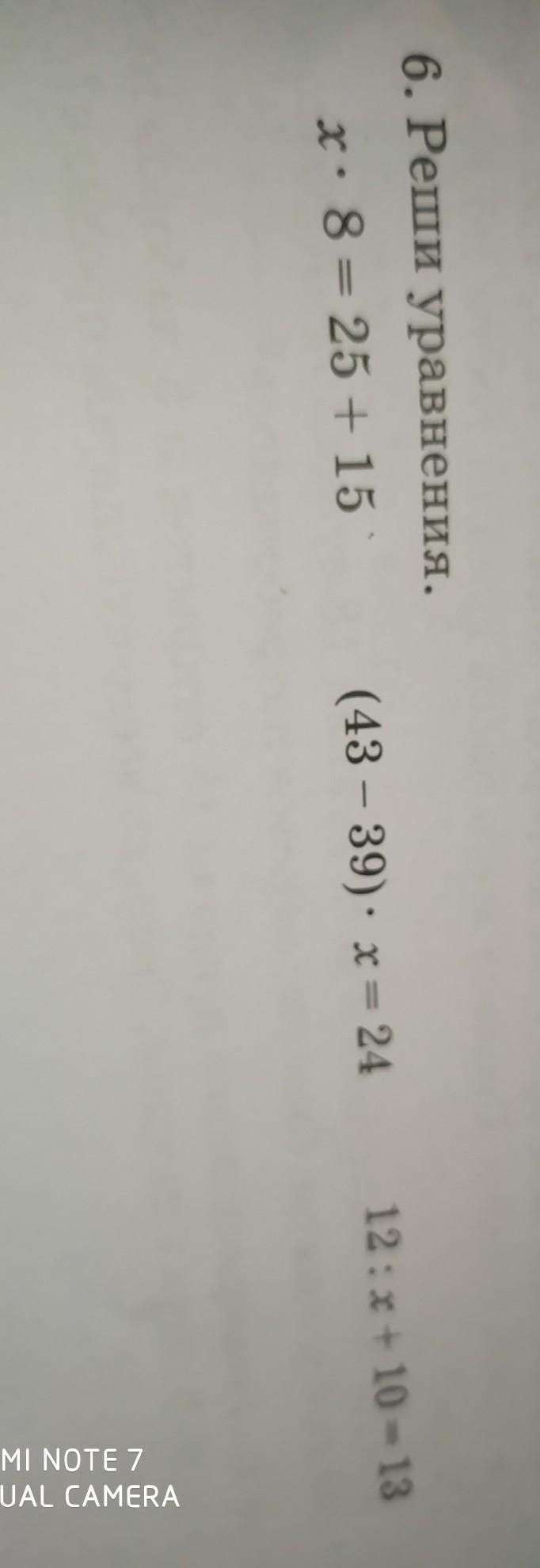
Ответы
Автор ответа:
10
Ответ:
12:x+10=13
12:x=13-10
12:x=3
X=12:3
X=4
Автор ответа:
3
x*8=25+15
8x=25+15
8x=40
x=5
Ответ: 5.
(43-39)*x=24
4x=24
x=6
Ответ: 6.
12:x+10=13
+10=13
12=3x
3x=12
x=4
Ответ: 4.
Интересные вопросы
Предмет: Русский язык,
автор: lisa190704
Предмет: Другие предметы,
автор: belnik80
Предмет: Другие предметы,
автор: davydyuk2211
Предмет: История,
автор: ko0tetkafadAn2ne
Предмет: Химия,
автор: NastikRbnLerkru