Предмет: Химия,
автор: rose2007
В результате сжигания 0.655 г вещества Х получили 0.385 г СО2 и 0.392 л(н.у) SO2. Определите молярную массу вещества Х.
Ответы
Автор ответа:
0
X+O2=CO2+SO2
C+O2=CO2 m(C)=12*0.385/44=0.105 гр n(C)=0.105/12=0.00875 моль
S+O2=SO2 m(S)=32*0.392/22.4=0.56 гр n(S)=0.56/32=0.0175 моль
n(C):n(S)=0.00875:0.0175=1:2 CS2
C+O2=CO2 m(C)=12*0.385/44=0.105 гр n(C)=0.105/12=0.00875 моль
S+O2=SO2 m(S)=32*0.392/22.4=0.56 гр n(S)=0.56/32=0.0175 моль
n(C):n(S)=0.00875:0.0175=1:2 CS2
Автор ответа:
0
..................................
Приложения:
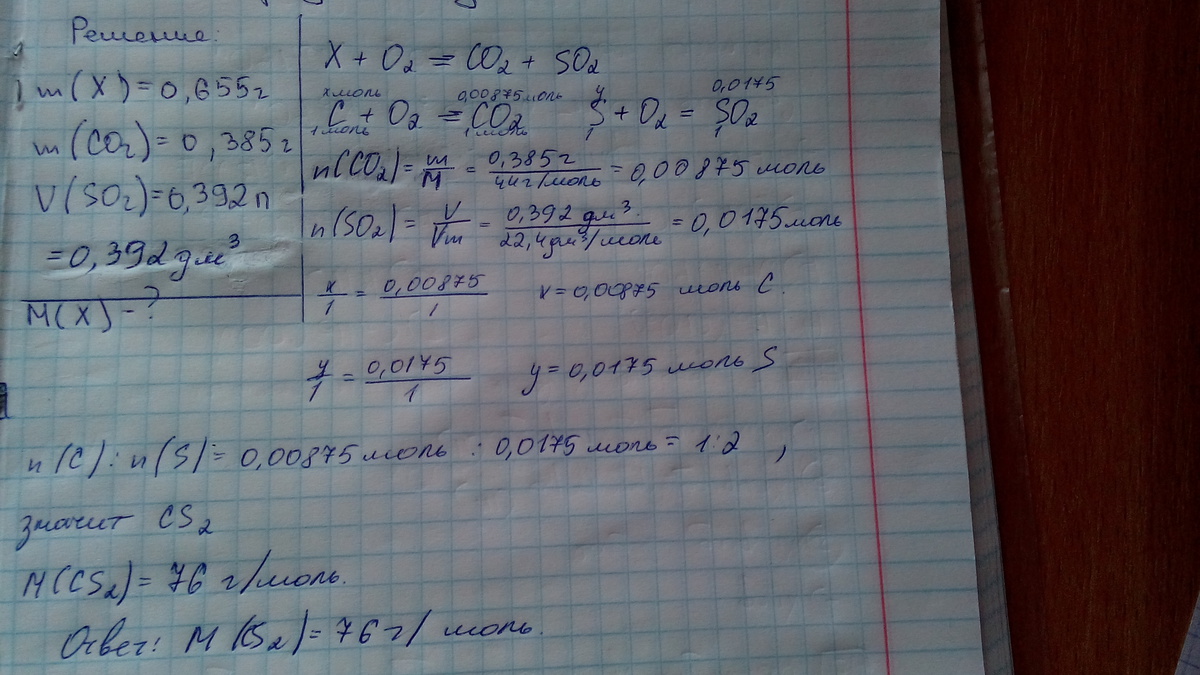
Интересные вопросы
Предмет: Математика,
автор: tokmukhammed
Предмет: Биология,
автор: radasakhi
Предмет: История,
автор: daaanizmajlovo
Предмет: Литература,
автор: siv76
Предмет: География,
автор: kondratenko1974